美国西北大学医学院的一项研究揭示了肌萎缩侧索硬化症(ALS)背后的关键分子机制,相关发现已发表于《Neuron》期刊。
该研究指出了细胞RNA "质量控制"系统的故障——该系统通常负责保持遗传信息的清洁和功能性。

"每个细胞都使用RNA作为信使,从DNA携带指令来制造蛋白质,但在ALS患者中,这些信息有时会出现错误或不完整,"该研究的资深作者、西北大学医学院神经病学系神经肌肉疾病和神经科学部门副教授Evangelos Kiskinis博士解释道。
"在大多数ALS患者中,我们知道一种主要位于细胞核内的RNA结合蛋白TDP-43会离开细胞核并在细胞质中形成聚集体,"Kiskinis说。"TDP-43的错误定位是疾病病理生理学的基础。在这项研究中,我们专注于理解TDP-43在人类运动神经元中的功能丧失如何影响RNA代谢。"
TDP-43与UPF1在ALS中的相互作用
在这项研究中,Kiskinis及其合作者检查了由诱导多能干细胞衍生的运动神经元。他们聚焦于UPF1,这是一种像校对员一样的蛋白质,负责扫描RNA并在有缺陷的副本引发问题之前将其清除。这个过程称为mRNA衰变,对健康细胞至关重要。
研究团队发现,UPF1和TDP-43通常协同工作来控制RNA信息的长度——尤其是在其尾部。这些区域有助于调节RNA信息的寿命及其在细胞中的去向。在ALS中,这些过程失控,导致RNA不稳定和神经元应激。
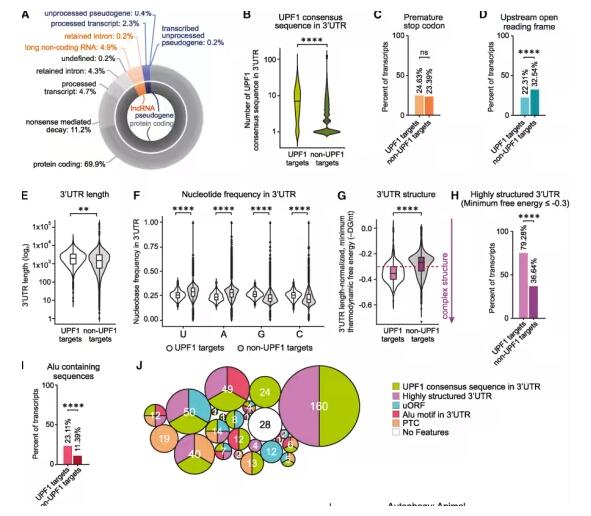
此外,研究发现,来自ALS患者的运动神经元以及TDP-43被耗竭的细胞中(TDP-43是ALS病理的标志性蛋白),UPF1的活性显著降低。研究证明,TDP-43的耗竭会破坏UPF1活性,并且这两种蛋白质以RNA依赖的方式相互作用,在ALS神经元组织中聚集在一起。
治疗意义与未来研究
"我们发现UPF1活性的降低,使得因TDP-43功能障碍而产生的错误RNA能够逃避正常的降解过程,并在病变神经元中积累,"Kiskinis实验室的博士后学者、该研究的第一作者Francesco Alessandrini博士说。"这就像双重打击,TDP-43和UPF1都不能很好地工作。"
这些发现揭示了RNA衰变、TDP-43功能障碍和神经退行性变之间此前未知的联系。
"既然我们已经识别出这些异常的RNA,我们的目标是理解它们在运动神经元崩溃中的作用,"Kiskinis实验室的研究数据分析师、该研究的合著者Matthew Wright表示。
这项研究不仅描绘了这个受损的RNA监视系统,还提出了新的治疗策略:如果科学家能够恢复UPF1的"校对"能力,他们或许可以减缓或阻止ALS造成的损伤。
"我们的这一发现对该疾病的病理生理学具有重要意义,"Kiskinis说。"如果这些RNA确实具有毒性,并且细胞无法承受,那么治疗上的启示就是,如果我们找到重新激活这一通路的办法,那显然将是有益的。"
参考文献:
Francesco Alessandrini et al, TDP-43 dysfunction compromises UPF1-dependent mRNA metabolism in ALS, Neuron (2025). DOI: 10.1016/j.neuron.2025.11.001.


