热门关键词: ELISA试剂盒 - 大鼠ELISA试剂盒- 小鼠ELISA试剂盒
全国统一客服热线:
0755-28715175
热门关键词: ELISA试剂盒 - 大鼠ELISA试剂盒- 小鼠ELISA试剂盒
全国统一客服热线:
0755-28715175
在肿瘤免疫研究中,抗原呈递始终是连接肿瘤细胞与免疫系统的核心环节。传统观点认为,HLA-II分子主要表达于树突状细胞、巨噬细胞和B细胞等专业抗原呈递细胞,而肿瘤细胞更多依赖HLA-I向CD8+ T细胞呈递抗原。
然而,近年来的大量临床与转录组数据表明,在黑色素瘤、肺癌等多种人类肿瘤中,癌细胞本身也可表达HLA-II,并且这种表达往往与更高的免疫细胞浸润水平、更好的免疫检查点抑制剂疗效以及更长的总生存期密切相关。
尽管这一现象已在多项研究和不同肿瘤类型中被报道,其背后的分子调控机制却始终未被系统阐明,尤其是在缺乏IFN-γ等炎症刺激的情况下,肿瘤细胞如何维持基础水平的HLA-II表达,仍是领域内的重要未解问题。
近日,北京大学定量生物学中心曾泽贤团队与罗春雄团队合作,在Journal of Experimental & Clinical Cancer Research (IF=12.8) 杂志上发表了题为The Aryl Hydrocarbon Receptor (AHR) Drives Human Leukocyte Antigen (HLA)-II Expression in Human Melanoma 的一项系统性研究。
通过全基因组CRISPR-Cas9筛选,该研究首次明确了芳烃受体AHR及其伴侣蛋白ARNT这一此前未被关注的调控轴,作为癌细胞固有HLA-II表达的关键正向调控因子,能够在不依赖IFN-γ的条件下直接驱动人类黑色素瘤细胞中HLA-II的组成型表达,为理解肿瘤细胞自身如何参与抗原呈递提供了新的分子框架。

研究人员首先利用全基因组CRISPR-Cas9筛选,在人源黑色素瘤细胞中系统鉴定了调控癌细胞HLA-II表达的关键因子。筛选以及功能验证显示,敲除AHR或ARNT会显著降低癌细胞表面HLA-II水平,表明AHR-ARNT通路是癌细胞固有HLA-II表达所必需的;而单独过表达任一因子,或在敲除背景下进行回补,均足以恢复甚至增强HLA-II的表达,进一步证明该通路不仅是必要条件,同时也是驱动HLA-II表达的充分条件。
配体刺激实验显示,AHR信号通路的激活能够以时间依赖且可逆的方式调控癌细胞HLA-II表达,这一动态特征提示AHR-ARNT通路具有潜在的药物可靶向性,并为未来AHR相关干预策略在肿瘤免疫治疗中的设计与给药时序优化提供了重要依据。
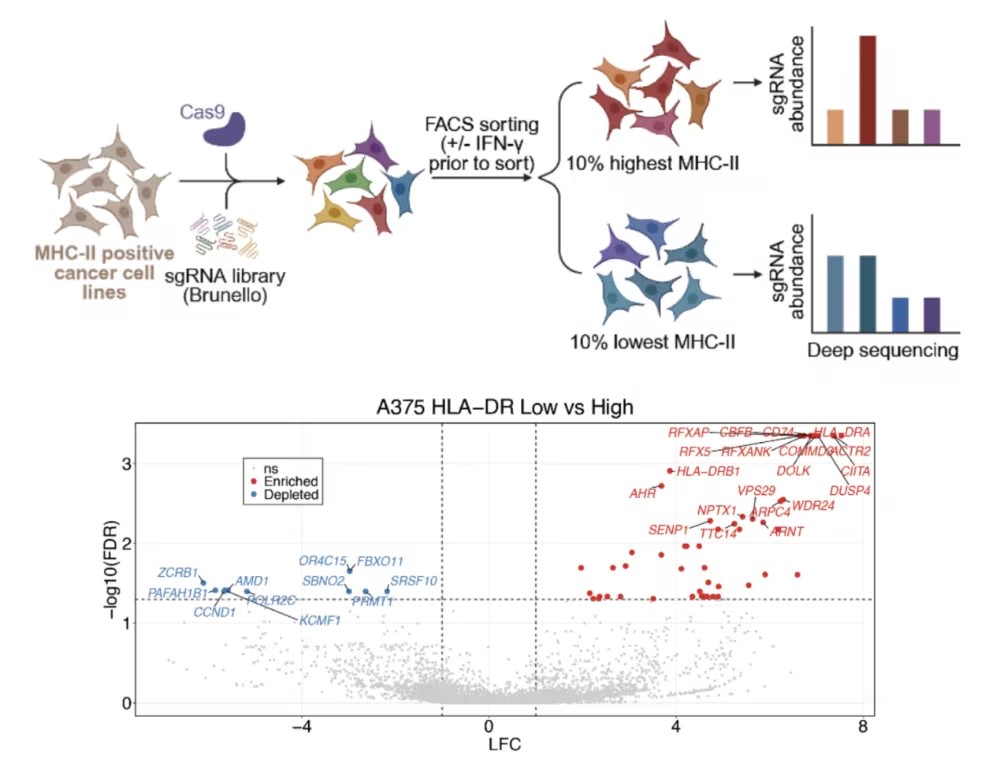
图1:全基因组CRISPR-Cas9筛选调控癌细胞HLA-II表达的关键因子
在分子机制层面,研究通过整合RNA-seq、ATAC-seq和ChIP-seq数据,首次明确了CIITA启动子pII在AHR-ARNT介导的癌细胞固有HLA-II表达中的关键作用。研究发现,AHR-ARNT复合物可特异性结合CIITA pII区域,并协调驱动CIITA多种转录本(II、III和IV型)的表达,从而激活下游HLA-II转录程序。这些结果首次明确了CIITA启动子pII在癌细胞固有HLA-II表达调控中的关键作用,并揭示了其在生理条件下的具体功能场景。
在此基础上,研究进一步构建了AHR-ARNT功能缺失特征,并在多癌种临床队列中分析其与肿瘤免疫微环境的关系及临床意义。结果显示,该特征与效应性免疫细胞浸润减少、免疫抑制性微环境增强显著相关。当与癌细胞HLA-II表达联合分析时,高HLA-II且AHR-ARNT功能相对完整的患者在黑色素瘤和肺腺癌中呈现出显著更好的生存获益。
0755-28715175/33164177

粤公网安备 44030902000304号