热门关键词: ELISA试剂盒 - 大鼠ELISA试剂盒- 小鼠ELISA试剂盒
全国统一客服热线:
0755-28715175
热门关键词: ELISA试剂盒 - 大鼠ELISA试剂盒- 小鼠ELISA试剂盒
全国统一客服热线:
0755-28715175
血管组织驻留巨噬细胞(VRMs)在血管中维持免疫平衡,但其在腹主动脉瘤(AAA)发生发展中的作用尚不明确。
2026年2月27日,复旦大学阮承超,庄涛,董智慧和上海交通大学陆炎,李燕共同通讯(陈梅华及滑艺杰为共同第一作者)在Nature Immunology 在线发表题为Sparcl1 mitigates abdominal aortic aneurysm through inhibiting lymphangiogenesis-mediated TLS formation的研究论文。该研究证实,位于血管外膜、以Lyve1表达为标志的一类特定VRMs,通过分泌细胞外基质蛋白Sparcl1(Sc1)发挥抗AAA作用。
在VRMs中敲除Sc1会促进功能异常的淋巴管生成,并导致三级淋巴结构(TLSs)形成,从而加速AAA进展。机制上,Sc1的钙结合结构域可捕获生长因子成纤维细胞生长因子2(FGF2),抑制FGF2介导的功能异常淋巴管生成以及与TLS形成相关基因的表达。
一种源自Sc1的治疗性多肽(Spa17)在多种AAA模型中均能缓解AAA进展。该研究揭示了VRM来源的Sc1在AAA中具有保护作用,并确定了一种潜在的治疗策略。
腹主动脉瘤(AAA)是一种危及生命的血管疾病,其特征是主动脉壁进行性扩张,破裂后死亡率极高。已确认的危险因素包括衰老、男性、高血压、高胆固醇血症、肥胖、吸烟及遗传易感性。目前主要依赖外科手术或血管内修复术进行治疗,这些方法具有侵入性,且伴随围手术期风险及再次干预的需要。这凸显了阐明驱动AAA发病的分子与细胞机制,以开发非侵入性疗法的迫切需求。
AAA的进展由多种病理机制驱动,包括细胞外基质(ECM)降解、血管平滑肌细胞(VSMC)丢失、氧化应激以及巨噬细胞等免疫细胞的浸润,这些因素共同削弱主动脉壁。巨噬细胞在此环境中起关键作用,通过分泌基质金属蛋白酶(MMPs)等蛋白酶和促炎细胞因子,促进ECM分解和VSMC功能障碍。
血管组织驻留巨噬细胞(VRMs)在维持动脉稳态中具有重要作用。VRMs是来源于卵黄囊和胎肝的组织驻留巨噬细胞,表达淋巴管内皮透明质酸受体1(Lyve1),并定位于机械应力较高的区域,在此处调节血管炎症、组织修复和VSMC存活。然而,VRMs在AAA进展中的作用尚不清楚。
血管ECM不仅是结构支架,更是一个动态的信号环境。ECM相关蛋白,如血小板反应蛋白、骨桥蛋白(OPN)和Sparc家族成员,是ECM的非结构组分,能够调节细胞信号传导和基质动力学,并被描述为炎症性疾病中血管重塑的调节因子。该家族成员Sparcl1(Sc1)与炎症和组织稳态相关,但其在血管疾病,特别是AAA中的作用尚不明确。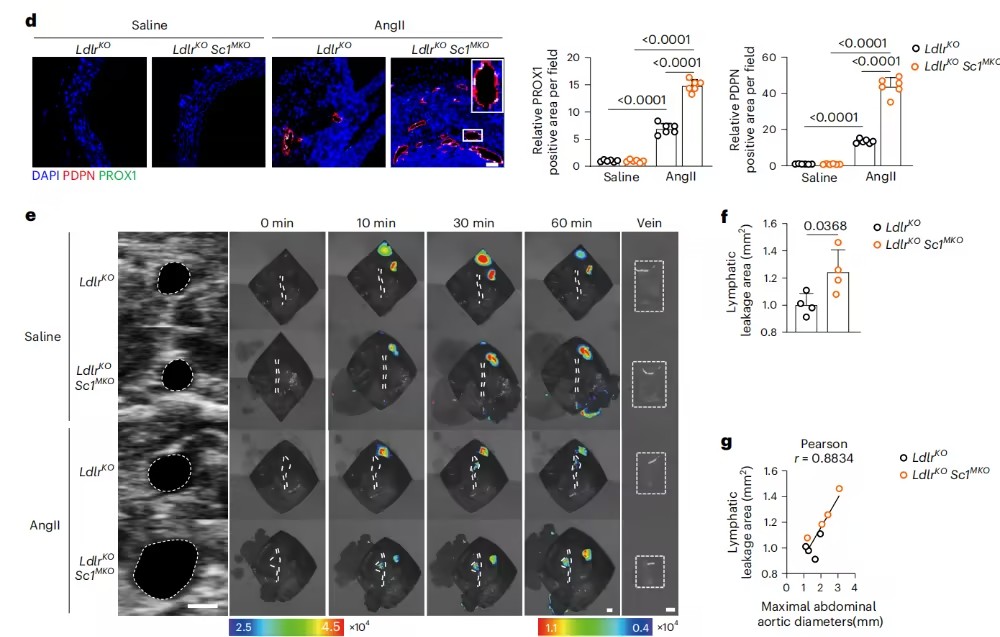
Sc1基因的VRM特异性缺失促进功能异常的淋巴管生成(图片源自Nature Immunology )
本研究探讨了VRM来源的Sc1在AAA中的功能。作者发现,Sc1通过阻断生长因子成纤维细胞生长因子2(FGF2),并抑制主动脉壁中功能失调的淋巴管生成及三级淋巴结构(TLS)形成,从而保护血管免受动脉瘤进展。
一种源自Sc1的治疗性多肽(命名为Spa17)在实验模型中减轻了AAA的进展。这些发现揭示了AAA发病机制中的一个保护性轴,并表明Sc1可能作为非侵入性治疗策略的开发基础。
0755-28715175/33164177

粤公网安备 44030902000304号