组织驻留型间充质基质细胞(MSC)可在损伤部位调控免疫细胞活化,这是组织修复过程中的关键事件。然而,驱动损伤应答性免疫–基质细胞相互作用的完整免疫调控机制仍有待深入阐明。
2026年3月7日,浙江大学闪波、杭州市第一人民医院黄进宇、浙江中医药大学吴颖、中国科学院邵孟乐共同通讯在Nature Communications在线发表题为“Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice”的研究论文。本研究利用小鼠血管内损伤模型,证实血管周间充质基质细胞可通过招募表达ST2的修复型巨噬细胞,增强雄性小鼠动脉的免疫应答。
时间序列单细胞测序结果显示,MSC介导的巨噬细胞表型转换对血管再生至关重要。机制上,损伤可激活MSC中依赖NFκB通路的IL‑33分泌,后者作为旁分泌信号,诱导ST2⁺巨噬细胞产生骨桥蛋白(OPN/SPP1),进而促进血管平滑肌细胞(VSMC)增殖与新生内膜形成。通过水凝胶局部递送靶向Il33或Spp1的siRNA,可有效缓解损伤诱导的新生内膜增生,提示这一策略有望用于预防再狭窄及其他血管疾病。本研究阐明了IL‑33–ST2–OPN轴介导血管周MSC与修复型巨噬细胞之间的功能性对话,从而调控免疫介导的修复反应。

组织修复可通过组织再生或瘢痕愈合两种方式完成。平衡良好的组织修复过程对于重建组织稳态至关重要,并决定疾病的发生发展。免疫细胞在调控组织修复必需的再生与炎症反应中发挥关键作用。组织损伤后,大量巨噬细胞被动员并激活,参与组织再生、炎症反应及纤维化进程。巨噬细胞以时序性、协同性的级联方式发挥作用,清除病原体或坏死碎片,并在组织损伤与修复过程中促进炎症消退。尽管巨噬细胞功能关键,但其修复型巨噬细胞的具体身份、谱系来源,以及调控其获得促修复表型的机制,仍不明确。
血管修复是一个受到严格调控的过程,其进程决定了血管损伤后内皮单层正常再生与病理性血管病变形成之间的微妙平衡。血管腔内损伤后,血管修复过程包括内皮细胞(EC)功能异常、血管平滑肌细胞(VSMC)增殖以及血管壁内活跃的免疫反应。内皮损伤可刺激血管平滑肌细胞增殖,并从中膜向内膜迁移,驱动称为新生内膜增生的血管重塑过程。然而,损伤应答性免疫反应的内在机制及其对血管平滑肌细胞增殖和新生内膜形成的影响,仍知之甚少。
免疫系统与微环境其他组分之间的复杂相互作用对组织修复与再生至关重要。损伤会触发多种免疫与非免疫细胞的募集、增殖和活化,共同构成细胞间通讯网络,协同调控组织修复。近期研究致力于阐明修复型巨噬细胞如何通过旁分泌/ 自分泌方式,产生细胞因子、生长因子、代谢物等生物活性因子,参与构建修复细胞微环境。已有研究报道多种细胞因子、生长因子及信号通路可调控巨噬细胞表型转换。值得注意的是,IL‑33/ST2信号通路可通过下游效应分子调控巨噬细胞及其他免疫细胞的表型,并在多种生理病理过程中发挥作用。但其在组织损伤与修复过程中巨噬细胞表型转换的作用仍不明确。
间充质基质细胞(MSC)是定位于血管周围区域的主要基质细胞,近期被证实为外周组织中IL‑33 的主要细胞来源。MSC 因其为组织器官提供结构支持的基础功能而被广泛认知。现已明确,MSC在组织修复中还具有额外功能,尤其是在损伤后激活免疫系统。在血管组织中,定位于外膜的外膜间充质基质细胞参与血管重塑及疾病发生相关通路。近期研究表明,MSC可通过与其他免疫细胞的双向相互作用响应损伤相关信号,动员多种对组织再生与伤口愈合至关重要的微环境组分。此外,细胞命运示踪与单细胞测序研究均证实,血管外膜是血管重塑的调控中心,可影响中膜与内膜细胞功能。值得注意的是,在钢丝诱导动脉损伤模型中,PDGFRβ⁺SCA1⁺外膜MSC 并不直接分化为新生血管平滑肌细胞,而是更可能以调控功能支持动脉修复过程,而非作为新生血管平滑肌细胞的细胞来源。
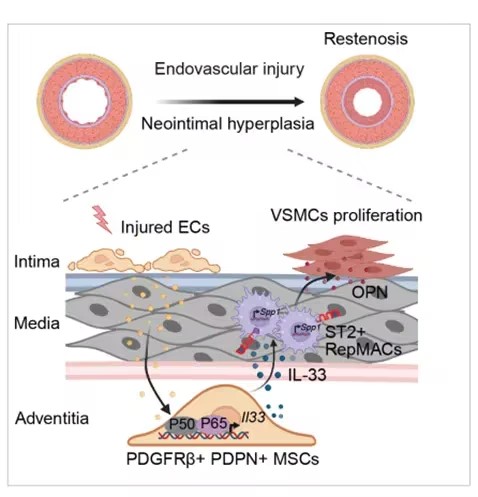
机制模式图(摘自Nature Communications )
在本研究中,结合时间分辨单细胞 RNA 测序与多色流式细胞术,全面分析血管壁内细胞间通讯网络的动态变化,并阐明血管腔内损伤后间充质基质细胞如何协调免疫反应。研究发现:间充质来源的 IL‑33 驱动 ST2⁺ 巨噬细胞活化,后者通过骨桥蛋白(OPN/SPP1)促进平滑肌细胞增殖与新生内膜形成;而阻断这一IL‑33–ST2–OPN轴可抑制新生内膜增生。上述结果为动脉修复过程中免疫‑基质细胞相互作用提供了机制框架,并为预防再狭窄及相关血管疾病提供了可靶向的治疗通路。


